老化のメカニズム
生体分子に起こる加齢変化
05-異常たんぱく質はなぜ増えるのか?
異常タンパク質のでき方
生体内では異常タンパク質はいろいろの原因で生じます。活性酸素による化学修飾(酸化修飾)もその一つです。
その他、グルコース(ブドウ糖)による化学修飾、熱(体温)によって起こる変性(立体構造変化)などがあります。まず多くのタンパク質の異常化に関わると考えられる酸化傷害について見てみましょう。
タンパク質はアミノ酸がじゅずつなぎに繋がった高分子で複雑に折りたたまれてそれぞれに特有の立体構造を形作っています。小さいタンパク質ではアミノ酸の数は数十個、大きいものになると数千個というのもあります。平均的なタンパク質だと数百というところです。いずれも立体構造が機能(例えば、酵素なら触媒活性、ヘモグロビンなら酸素結合性など)にとって重要です。立体構造は熱が加わったり、構成アミノ酸が化学修飾を受けると変化して機能が低下したり、失われたりします。
ここでは多くのタンパク質の異常化に関わると考えられる酸化傷害について見てみましょう。
タンパク質が活性酸素に出会うと、主に、そのアミノ酸単位(アミノ酸残基)から出ている側鎖部分が活性酸素と反応して種々の化学変化を起こします。化学変化を起こしやすい部分は、機能にかかわりの深いことが多いので生じた酸化修飾タンパク質は、本来の機能を失ってしまう可能性が高いのです。
タンパク質異常化の指標によく使われる酸化修飾構造の一つにカルボニル基があります。カルボニル基は、特にリシンやアルギニンといったアミノ酸残基の側鎖が酸化されて出来やすいとされています。
もう一つ、タンパク質異常化の原因にはブドウ糖(グルコース)による修飾があります。活性酸素による酸化修飾が主に細胞内で起こるのに対して、ブドウ糖による修飾は主に細胞外のタンパク質に対して生じます。一般に細胞内に入ったブドウ糖はすぐに代謝されてしまうためと、細胞内タンパク質は代謝回転が早いため修飾体が蓄積しにくいのです。糖尿病の指標に使われるヘモグロビンA1Cは赤血球内のヘモグロビンがブドウ糖と反応した結果できた修飾体です。血糖値が高ければそれだけ多く修飾されます。赤血球の寿命が長く(ヒトでは120日)ヘモグロビンも長く赤血球中に留まっているため修飾体が蓄積するのです。
ブドウ糖はエネルギー源として最も重要な物質で食後を別にして血中のレベル(血糖値)は常に一定範囲に保たれています。低血糖になるとエネルギー不足(特に脳)で意識を失ったり、死亡したりすることもあり大変危険です。一方、糖尿病では食後の高血糖がいつまでも下がりません。そのためブドウ糖によるタンパク質修飾のために糖毒性が生じ、これが長く続くと糖尿病合併症(網膜症、神経症、腎疾患など)が発症することになります。糖尿病は病的老化を促進すると考えられ、早老症とみなす研究者もいます。
異常タンパク質の分解
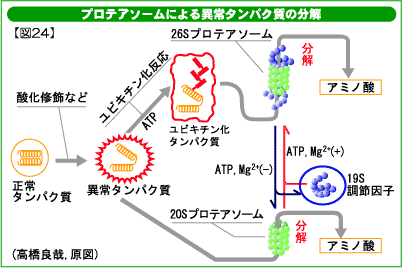
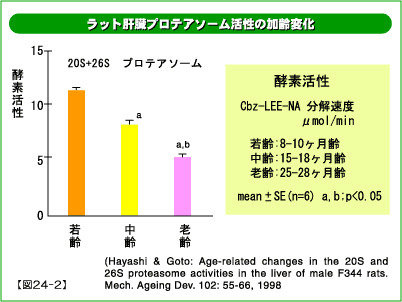
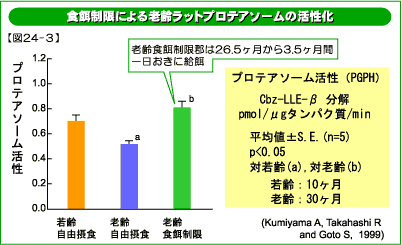
異常タンパク質は、一般に図24に示すようにプロテアソームと呼ばれるタンパク質分解酵素によって分解されると考えられています。二種類のプロテアソーム(26Sと20Sプロテアソーム)は、どちらも多数のタンパク質分子からなる巨大分子量の複合体です。多くの異常タンパク質は、ユビキチン化を受けたあと26Sプロテアソームによって分解されると考えられています。酸化タンパク質は20Sプロテアソームでも分解されます。図24−2は、ラット肝臓のプロテアソーム活性の加齢変化です。老齢動物で活性が低下していることが分かります。
異常タンパク質蓄積の原因:タンパク質代謝回転の低下
生物の身体を構成するタンパク質は、遺伝子の指令で合成されますが、いつまでも一定不変で細胞の中に留まっているのではなく、しばらくすると分解され、再び合成されるという動的なサイクルを繰り返しています。合成と分解という動的なサイクルを代謝回転と言います(図16)。
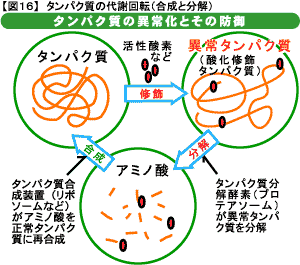
このダイナミックな物質の動きは、生命の維持に大変重要です。なぜなら細胞内で常に生じている異常タンパク質を除去し、分解によって生じたアミノ 酸を再利用しなければ、やがて細胞は機能しなくなってしまうでしょう。また、細胞内外の変化に応じて要らなくなったタンパク質を壊し、必要なタンパク質を作らなくてはなりません。動物が歳を取ると細胞のタンパク質生合成活性も低下します。したがって高齢動物では代謝回転が遅くなっていることになります。
分解効率は、分解半減期や分解酵素の活性から推定することが出来ますが、私たちや他の研究者によって老齢動物の細胞ではタンパク質の分解半減期が延び、壊れにくくなることが明らかにされています(下図26)。
【図26-2】培養した老若マウスの肝臓細胞に卵白リゾチームあるいは酸化修飾した卵白リゾチーム(異常タンパク質のモデル)を導入して時間を追って分解を調べました。
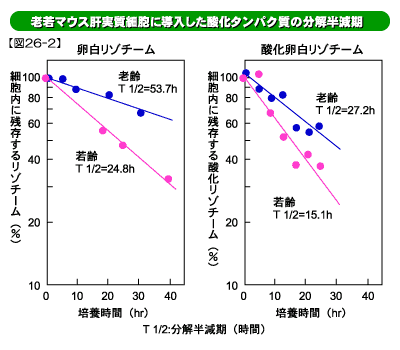
分解は一次反応に従って起こり、分解半減期(![]() )を算出できます。両タンパク質とも老齢動物の細胞では分解半減期が延びている、すなわちタンパク質が分解されにくくなっていることが分かります。
)を算出できます。両タンパク質とも老齢動物の細胞では分解半減期が延びている、すなわちタンパク質が分解されにくくなっていることが分かります。
![]() 卵白リゾチームの分解半減期:老齢53.7時間、若齢24.8時間
卵白リゾチームの分解半減期:老齢53.7時間、若齢24.8時間
![]() 酸化卵白リゾチームの分解半減期:老齢27.2時間、若齢15.1時間
酸化卵白リゾチームの分解半減期:老齢27.2時間、若齢15.1時間
細胞内のタンパク質分解酵素:その加齢変化
タンパク質の分解半減期が延びるのは、分解酵素の活性が低下することによる可能性があります。
タンパク質分解酵素というと胃のペプシンや腸のトリプシンなどがよく知られていますが、いずれも細胞外に分泌される消化酵素です。細胞内にも、カテプシン・プロテアソーム・カルパインなど何種類ものタンパク質分解酵素が存在します。
このうち主要な異常タンパク質分解酵素であるプロテアソームの活性は、老齢動物で低下します(図24-2)。
他のタンパク質分解酵素は、活性があまり変わらないか、逆に増えるものもあります。
私たちの研究室では老齢動物のプロテアソームの活性を阻害すると異常タンパク質の分解も抑えられることを明らかにしています。興味深いことにプロテア ソームの活性低下は、酵素の量が減ったためではなく、酵素自身が異常化しているためのようです。異常タンパク質を分解除去する酵素自身が異常化すれば、他の異常タンパク質の分解が遅くなってしまうのはうなずけます。
![]()