老化介入・老化制御
摂取カロリーと老化
“NMNは夢の若返りサプリメント?”
NMN(エヌエムエヌ):これは、昨年(2015年)の正月4日のNHKスペシャル番組『私たちの未来Next World』で放送され、若返りを実現出来るかもしれないというふれ込みで注目を浴びた物質です。ニコチンアミド モノヌクレオチド(nicotinamide mononucleotide)を省略してNMNと書きます。正月休み中の放送で若返りというメデタイ話なので注目度も高かったようで、何人かの友人に、あれは本当なの?と尋ねられました。以前(2011年8月30日掲載)にも同種の番組についてこの欄で解説していますので(「レスベラトールの寿命延長・抗老化作用についての見解」を参照)、今回の件についても私見を述べたいと思います。
細胞内で遺伝情報に基いて合成(翻訳という)されたタンパク質の多くは、色々な化学的な変化を受けています(翻訳後修飾という)。翻訳後修飾によって機能のあるかたちになったり、修飾を解除して機能がないかたちに戻ったりしながら、状況に応じて変化して細胞機能の維持に関わっています。よく知られているものにリン酸化があります。タンパク質のリン酸化・脱リン酸化はノーベル生理医学賞の対象にもなった重要な生体恒常性維持機構の一つです。その異常はがん化やアルツハイマー病にも関わっています。
こうした翻訳後修飾の一つにアセチル化があります(表1)。
| −翻訳後装飾− | |
|---|---|
| 生理的 | リン酸化・脱リン酸化 |
| アセチル化・脱アセチル化 | |
| 糖鎖付加 | |
| 非生理的 | 酸化(カルボニル化など) |
| 糖化 |
(註)
生理的修飾は酵素の働きによって起こり、生体調節機能に関わっている。非生理的修飾は主に酵素に依存しないで起こり、タンパク質の本来の機能を失わせたり、有害な働きをもつものに変えてしまう場合が多い。糖化はタンパク質とブドウ糖が酵素を介さないで反応することによって起こり、一般にも知られるようになったAGE(advanced
glycation endproducts) と総称される種々の修飾産物を生じる。
アセチル化は、タンパク質中のアミノ酸残基(タンパク質を構成しているアミノ酸、タンパク質の大きさによって通常数百から数千個ある)の中のリシンというアミノ酸残基に起こります。アセチル化修飾を受けるタンパク質は沢山ありますが(2000種類以上)、修飾によってタンパク質の機能が高まったり、抑えられたりします。修飾を受けるリシン残基は、同じタンパク質の中の一つであったり複数であったりします。どの残基がアセチル化されるかで、活性に与える影響が異なります。
アセチル化を触媒する酵素(protein acetyl transferase,タンパク質アセチル基転移酵素、ここでは略してアセチル化酵素)は複数あります(図1)。この酵素はブドウ糖や脂肪酸などに由来するアセチル基(図1に示すようにアセチルCoAという形になっている)をタンパク質に結合する反応を触媒します(酵素の触媒作用の説明は「抗老化・酵素健康法の真偽」参照)。なお、非酵素的なタンパク質のアセチル化も知られていてタンパク質機能を阻害する要因の一つで、後述のサーチュインは、それを防ぐ機構だという主張もあります。
一方、タンパク質に結合したアセチル基を取り除く酵素(protein deacetylase, タンパク質脱アセチル化酵素)もあり、これも複数種類あって、タンパク質の種類や存在場所(核やミトコンドリアなど)に応じて特定の酵素が働きます。
このようにアセチル化・脱アセチル化に関わる酵素には多くの種類があり、アセチル化・脱アセチル化を受けるタンパク質(標的タンパク質という)も多種類あります。これらの酵素や標的タンパク質は細胞や生体の状況に応じて微妙に変化して生体の恒常性維持に関わっていると考えられています。
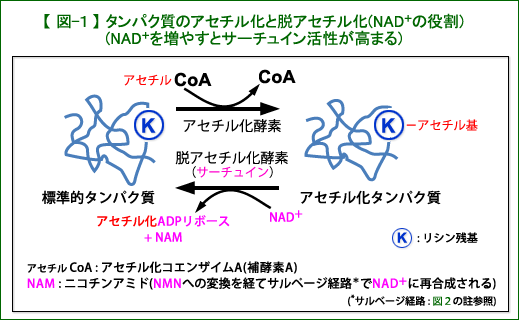
脱アセチル化酵素の中で、上記のNHK番組に出てきたサーチュイン(Sirtuin:SIRT)と呼ばれる一群の酵素は、その作用のために取り外したアセチル基の受け取り手を必要とします。受け取り手はNAD(nicotinamide adenine dinucleotide, ニコチンアミドアデニンジヌクレオチド; 細胞内ではプラス荷電をもつためしばしばNAD+と書かれる。英語の省略形にプラス記号を付けるのは奇異な感じがするが、ここでは慣習にしたがってNAD+と書くことにする)と呼ばれる小さな分子です。サーチュインは、NAD+がないと作用を発揮出来ません。酵素(サーチュイン)量が同じならNAD+濃度が高い方がアセチル基の受け取り手が増えて、より強い脱アセチル化作用をもつことになります。当然、アセチル化の素材であるアセチルCoA(図1)の量もアセチル化の程度を左右する要因です。
一般にサーチュイン作用が強く、したがってタンパク質の脱アセチル化が促進されると、標的タンパク質の機能が高まって生体にとって好都合な変化を起こすといわれています。たとえば、抗酸化系酵素遺伝子の発現を高める、炎症性タンパク質遺伝子の発現を抑える、など。しかし、標的タンパク質がDNA結合タンパク質のヒストンの場合は状況によって影響は異なります。なお、エネルギー産生に関わる酵素の中には脱アセチル化で機能が低下するものもあります。
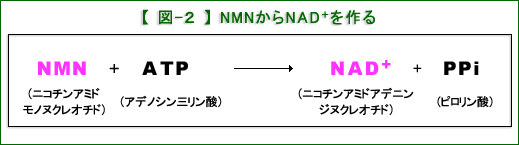
NMNは細胞内でNAD+を作る際の材料です(図2)。したがってNMNを増やしてやれば、NAD+が増えてサーチュインの作用が高くなると予想されます。なお、NAD+は、生体エネルギー(ATP)を作る際にもエネルギー源(ブドウ糖や脂肪酸など)から水素原子を受け取るという生命の根幹にかかわる反応に必要です(この場合は補酵素と呼ばれます。”脂肪を燃やす”を参照)。NAD+は、さらに、傷害を受けたDNAの修復にも必要で、たいへん重要な物質です。
註
NAD+が作られる生体内経路は基本的に二通りある。ひとつは、原材料(アミノ酸のトリプトファン)から作られるもので新規合成経路(デ・ノボ経路)とよばれる。もう一つは、上に書いたようにNMNなどを使った再利用経路(サルベージ経路)である。NMNは生体内でNAD+の代謝産物として生じ、それを再利用してNAD+を作ることが出来る。サルベージ経路は一般に沈没船を引き上げてその中の材料を使って船を造るのに似ているという意味からそう呼ばれる。この経路はデ・ノボ経路より反応段階が少なく、手間をかけずに、より簡単にNAD+を作ることができる。トリプトファンはタンパク質の材料であると同時に神経伝達物質など生体に必要な他の物質を作るのにも使われるので、それを使ってデ・ノボ経路でNAD+を増やそうとするのは得策でない。
哺乳類には7種類のサーチュイン(SIRT1-7)が知られています。それぞれ標的タンパク質が違いますが、NMN投与でNAD+が増加すれば、複数のサーチュインが影響を受ける可能性があります。ただし、それぞれのサーチュインが存在する細胞内の場所(核・ミトコンドリア・細胞質)が違う上にそれぞれの場所のNAD+濃度も異なり影響は同じではないと考えられます。
細胞のサーチュイン活性を高めるもうひとつの方法は、サーチュイン自体を増やしてやることです。2011年のNHKスペシャル番組に出てきたのは、種々の動物で寿命延長や抗老化作用があるカロリー制限やレスベラトール摂取でサーチュイン量が増加するという話でした。ヒトと同じ哺乳類のマウスを使った研究では、レスベラトールにサーチュイン増加作用も寿命延長作用も見られないことが明らかになっています。ヒトでは私の知る限り、この点に関する信頼できる報告はありません(「レスベラトールの寿命延長・抗老化作用についての見解」を参照)。カロリー制限ではマウスで一部のサーチュインが増加すると報告されています。では、NMNはどうでしょうか。
サーチュイン活性の増加に抗老化・寿命延長作用があるなら、サーチュイン量が増えなくても、その活性に必要な物質(NAD+)を増やしてやれば、同様の効果が期待できそうです。
ワシントン大学の今井眞一郎博士らはNMNをマウスに投与して、その影響を調べました。その結果が2015年正月のTV番組で紹介されたというわけです。彼らの報告(1)によると、高脂肪食によって糖尿病症状を起こさせたマウスにNMNを一週間(メスの場合)あるいは10日間(オスの場合)毎日投与(体重1 Kgあたり一日500mgを腹腔内注射)すると、各種の指標で病態改善を示唆する変化が見られました。オスとメスでは応答が異なっていて、オスでは高脂肪食の影響は加齢変化と同様で(高齢で一部の個体が糖尿病を発症する)、肝臓と白色脂肪組織(いわゆる腹部脂肪)でNAD+濃度の低下が見られました。それがNMN投与で回復(上昇)しました。NMN投与によってNAD+が増加しサーチュイン(SIRT1)作用が高まれば、標的タンパク質の脱アセチル化が亢進する可能性があります。
実際、標的タンパク質のNF-kB(p65)のアセチル化が減少しました。NF-kBには炎症に関わるタンパク質の発現(遺伝子から情報を読み取り、その情報を元にタンパク質を合成)を促進する働きがあり、アセチル化されると活性が高まります。したがってSIRT1によって脱アセチル化が起こると、NF-kB作用が弱まり、炎症が抑制されて糖尿病の進行に歯止めがかかるというストーリーが成り立ちそうです。こうしてNMNは高脂肪食マウスの糖尿病症状の改善に役立っているというわけです。
しかし、普通の食事をしているヒトの糖尿病を改善したり、予防したり、その他の病気の発症を抑えたり、老化そのものを遅らせて健康長寿に役立ったりするかどうかはわかりません。前述のようにNMNからできるNAD+は多くの重要な代謝反応に関わっていることを考えると、NAD+を長期にわたって人為的に増やすと予期しないマイナス作用が出るかもしれません。マウス実験の投与量を体重60 Kgのヒトに換算すると一日30グラムという膨大な量になりますから、このレベルの量をヒトに投与するとなると、その悪影響が懸念されます。
2011年以降、NMNの長期投与の影響に関する学術誌への報告は無いようです(2015年12月15日現在)。同グループの報告では、マウスの脳下垂体(成長ホルモン、オキシトシン、甲状腺ホルモンなど各種ホルモンを分泌する組織)だけでSIRT1の発現を高める遺伝子操作をほどこすと寿命がメスで16%、オスで9%ほど伸びたということです(2)。別のグループの研究では、同様の遺伝子操作で全身のSIRT1を増加させた場合は、寿命の変化は見られなかったといいます(3)。注意していただきたいのは、両研究はSIRT1の発現を組織特異的に、あるいは全身で高めたもので、NMN投与の影響をみたものではありませんから、外来のNMNの寿命延長作用については不明だという点です(放送のあとのインターネットニュースに”メスのマウスにNMNを投与したら寿命が16%延びる・・・60歳の人が20歳に若返る”などという原報(1),(2)には無い記述がありました(http://www.excite.co.jp/News/odd/Tocana_201501_post_5522.html)。16%の寿命延長が報告されているのはサーチュイン(SIRT1)の強制高発現マウスです。脳下垂体特異的なSIRT1活性上昇が長寿に役立つとしても、NMNで全身のSIRT1活性が高まった場合、寿命延長効果はみられるかどうかは分かりません。
老化と寿命(aging and longevity)は、しばしば並べて用いられ、時に同一視されることがありますが、両者には関連はあるものの、別物です。したがってNMNに寿命延長作用がなかったとしても抗老化作用もないことにはなりません。上に引用した論文では、高脂肪食マウスでは幾つかの指標でNMNに抗老化作用がある可能性を示唆しています。NMN投与によって、たとえば、糖耐性(ブドウ糖の利用(細胞取り込みや代謝)が低下した状態)を軽減したり、インスリン感受性を高めたり、炎症反応の抑制、酸化ストレス防御系酵素遺伝子の発現亢進などを引き起こすと報告されています(1)。しかし、この結果は、通常食の高齢動物あるいはヒトで観察されものではありませんから、生理的老化に対する影響がどうなるかは、今後の課題といえるでしょう。
NMNは、放送から何ヶ月経っても新聞記事に登場したりして(例えば2015年10月23日発行産経新聞 http://www.sankei.com/life/news/151023/lif1510230013-n1.html)、注目度はあいかわらず高いようですが、初夢が目出度く正夢になるか、白昼夢に終わるのか、研究の展開を見守りたいと思います。
- (1) Yoshino J et al. Nicotinamide mononucleotide, a key NAD+ intermediate, treats the pathophysiology of diet-and age-induced diabetes in mice. Cell Metabol 14: 5-14, 2011
- (2) Satoh A et al. Sirt1 extends life span and delyas aging in mice through the regulation of Nk2 homeobox 1 in the DMH and LH. Cell Metabol 18:416-430, 2013
- (3) Herranz D et al. Sirt1 improves healthy ageing and protects from metabolic syndrome-associated cancer syndrome. Nat Commun 1: 3.doi:10.1038/ncomms1001
![]()
