|
|
|||||
 |
搶朚戝妛丂栻妛晹栻暔妛嫵幒丂丂
揷拞 岝丂峴曽 堖桼婭丂鸐岥惓屽 |
||||
丂 怱憻偺昦婥偲帯椕栻丂|丂僄儂僯僕僺儞暔岅丂|丂僾儘僼傿亅儖丂|丂
 柶愑帠崁丂乥
柶愑帠崁丂乥怱憻偺廂弅
![]() 怱嬝偺旝嵶峔憿丂
怱嬝偺旝嵶峔憿丂![]() 僇儖僔僂儉僀僆儞偑怱憻傪摦偐偟偰偄傞
僇儖僔僂儉僀僆儞偑怱憻傪摦偐偟偰偄傞
丂![]() 怱嬝嵶朎撪僇儖僔僂儉僀僆儞偺崅懍僀儊乕僕儞僌丂
怱嬝嵶朎撪僇儖僔僂儉僀僆儞偺崅懍僀儊乕僕儞僌丂![]() 怱嬝廂弅偺摿惈
怱嬝廂弅偺摿惈
僇儖僔僂儉僀僆儞偑怱憻傪摦偐偟偰偄傞両
擄堈搙俀
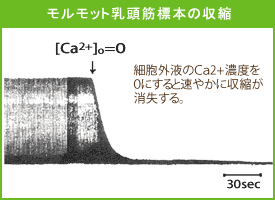
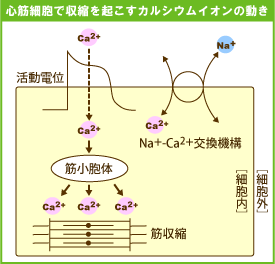
| 怱嬝嵶朎枌偺妶摦揹埵偑堷偒嬥偲側偭偰嬝廂弅偵帄傞夁掱乮 嫽暠亅廂弅娭楢丄俤亅俠 coupling 乯偵偼丄嵶朎奜偐傜嵶朎枌傪捠偭偰棳擖偡傞僇儖僔僂儉僀僆儞乮俠倎俀亄乯偑廳梫側栶妱傪墘偠偰偄傞偲峫偊傜傟偰偄傞偺偱偡丅 偙偺偙偲偼丄怱嬝昗杮傪怹偡梟塼乮 嵶朎奜塼 乯偐傜俠倎俀亄傪彍嫀偡傞偲丄妶摦揹埵偼婲偙偭偰偄偰傕怱嬝廂弅椡偼嬌傔偰抁帪娫偵徚幐偡傞偲偄偆娙扨側幚尡偐傜傕梕堈偵悇應偱偒傑偡乮塃恾丄忋乯丅 怱嬝嵶朎偵妶摦揹埵偑敪惗偡傞偲僇儖僔僂儉僠儍僱儖偑奐岥偟丄俠倎俀亄偑嵶朎撪偵棳擖偟傑偡丅棳擖偟偨俠倎俀亄偼嬝彫朎懱乮sarcoplasmic reticulum; 俽俼乯偺junctional SR偺儕傾僲僕儞庴梕懱僠儍僱儖乮ryanodine receptor僠儍僱儖丟俼倄俼俠乯傪奐岥偝偣丄偦偙傪捠偭偰戝検偺俠倎俀亄偑俽俼撪偐傜嵶朎幙偵曻弌偝傟傑偡丅偙偺俠倎俀亄偵傛傞俼倄俼俠偐傜偺俠倎俀亄曻弌懀恑偼俠倎俀亄-induced -俠倎俀亄 release 乮CICR乯偲屇偽傟偰偄傑偡丅嵶朎撪偺俠倎俀亄偼廂弅僞儞僷僋偵寢崌偟偰廂弅傪堷偒婲偙偟偨屻丄嵞傃SR偵庢傝崬傑傟傞偐嵶朎枌忋偺俶倎亄-俠倎俀亄岎姺婡峔偵傛傝嵶朎奜傊偲偔傒弌偝傟傑偡丅偙偺廂弅帪偺嵶朎幙撪俠倎俀亄擹搙偺忋徃偲掅壓偺摦偒偼俠倎俀亄僩儔儞僕僃儞僩偲屇偽傟偰偄傑偡丅妶摦揹埵偺敪惗偡傞慜偼栺侾侽侽値倣偱偡偑丄俠倎俀亄僩儔儞僕僃儞僩偺僺乕僋偱偼侾儅僀僋儘儊乕僩儖埲忋偵側傝傑偡丅 偙偺傛偆偵怱嬝偺廂弅偼俠倎俀亄僩儔儞僕僃儞僩偵傛傝惂屼偝傟偰偄傞傢偗偱偡偑丄僇儖僔僂儉姶庴惈寀岝僾儘乕僽偲偄偆摿庩側暘巕傪梡偄傞偲偙偺僇儖僔僂儉僀僆儞偺曄壔傪栚偱尒傞偙偲偑壜擻偱偡丅僇儖僔僂儉姶庴惈寀岝僾儘乕僽偵偼僇儖僔僂儉僀僆儞擹搙偺曄壔偵墳偠偰寀岝傪弌偡惈幙偑偁傝傑偡丅偙傟傪惗偒偨怱嬝嵶朎偵偁傜偐偠傔庢傝崬傑偣偰偍偒丄嫟徟揰儗乕僓乕尠旝嬀偱娤嶡偡傞偲丄妶摦揹埵偺敪惗捈屻偵嵶朎幙慡懱偺僇儖僔僂儉僀僆儞擹搙偑忋徃偟丄偦偺偁偲偵嵶朎偺廂弅偑婲偒偰偄傞偙偲偑傢偐傝傑偡丅偙傟偑怱憻偺慡偰偺怱嬝嵶朎偱傎傏摨帪偵婲偙傞偺偑惓忢偺怱嬝廂弅偱偡丅偮傑傝丄怱憻偑惓偟偔攺摦偡傞偨傔偵偼偙偺"妶摦揹埵仺俠倎俀亄僩儔儞僕僃儞僩仺廂弅"偺偟偔傒偑惓偟偔嶌摦偡傞昁梫偑偁傝傑偡丅偙偺棳傟偺偳偙偐偵堎忢偑惗偠傞偲怱憻偺攺摦偑晄婯懃偵側傞忬懺丄偡側傢偪晄惍柆偲側傝傑偡丅 僇儖僔僂儉姶庴惈寀岝僾儘乕僽偲嫟徟揰尠旝嬀傪慻傒偁傢偣偨庤朄偵傛傝丄惗偒偨怱嬝嵶朎撪偺僇儖僔僂儉偺摦偒傪偝傜偵徻偟偔抦傞偙偲偑弌棃傑偡丅傑偨丄寀岝僾儘乕僽偵偼僇儖僔僂儉僀僆儞偵尷傜偢丄奺庬嵶朎撪暔幙傗僞儞僷僋婡擻傪懆偊傞偨傔偺傕偺偑師乆偲峫埬偝傟偮偮偁傝丄條乆側惗柦尰徾偺棟夝傗帯椕栻奐敪傊偺墳梡側偳丄柌偼柍尷偵峀偑傝傑偡丅 偙傟傜偺婡峔傪柾幃揑偵恾偵帵偟傑偡乮塃恾丄壓乯丅 |
 |
|
廂弅僞儞僷僋偲僇儖僔僂儉僀僆儞
墶栦嬝嵶朎乮崪奿嬝嵶朎偲怱嬝嵶朎乯偺拞偵傾僋僠儞傪庡惉暘偲偡傞嵶偄慇堐偲儈僆僔儞傪庡惉暘偲偡傞懢偄慇堐偲偑娷傑傟偰偄傑偡丅墶栦偑尒偊傞偺偼偙傟傜偺慇堐偑婯懃惓偟偔暲傫偱偄傞偐傜偱偡丅妶摦揹埵偑敪惗偟丄嵶朎幙撪偺僇儖僔僂儉僀僆儞擹搙偑崅傑傞偲偙傟傜俀庬偺慇堐偑偍屳偄偺娫偵妸傝崬傓傛偆偵堏摦偟丄嵶朎偑弅傒傑偡丅偙傟偑嬝擏偺廂弅偺偟偔傒偱偡丅嬝廂弅偺嫮偝偼僇儖僔僂儉僀僆儞擹搙偺忋徃偺掱搙偵墳偠偰曄壔偟傑偡丅廬偭偰丄嬝擏偺廂弅偺昿搙傗嫮偝傪惂屼偡傞偵偼廂弅僞儞僷僋偵嶌梡偡傞僇儖僔僂儉僀僆儞偺擹搙曄壔乮俠倎俀亄僩儔儞僕僃儞僩乯傪挷愡偡傟偽傛偄傢偗偱偡丅帠幚丄懡偔偺惗懱撪妶惈暔幙傗栻暔偑俠倎俀亄僩儔儞僕僃儞僩偵塭嬁偟偰丄嬝廂弅偵塭嬁傪梌偊偰偄傑偡丅
