|
|
|||||
 |
搶朚戝妛丂栻妛晹栻暔妛嫵幒丂丂
揷拞 岝丂峴曽 堖桼婭丂鸐岥惓屽 |
||||
丂 怱憻偺昦婥偲帯椕栻丂|丂僄儂僯僕僺儞暔岅丂|丂僾儘僼傿亅儖丂|丂
 柶愑帠崁丂乥
柶愑帠崁丂乥怱憻偺廂弅
![]() 怱嬝偺旝嵶峔憿丂
怱嬝偺旝嵶峔憿丂![]() 僇儖僔僂儉僀僆儞偑怱憻傪摦偐偟偰偄傞
僇儖僔僂儉僀僆儞偑怱憻傪摦偐偟偰偄傞
丂![]() 怱嬝嵶朎撪僇儖僔僂儉僀僆儞偺崅懍僀儊乕僕儞僌丂
怱嬝嵶朎撪僇儖僔僂儉僀僆儞偺崅懍僀儊乕僕儞僌丂![]() 怱嬝廂弅偺摿惈
怱嬝廂弅偺摿惈
怱嬝嵶朎撪僇儖僔僂儉僀僆儞偺崅懍僀儊乕僕儞僌
擄堈搙俁
俠倎俀亄僩儔儞僕僃儞僩丂乮僇儖僔僂儉僩儔儞僕僃儞僩乯
俠倎俀亄僂僃乕僽丂乮僇儖僔僂儉僂僃乕僽乯
俠倎俀亄僗僷乕僋丂乮僇儖僔僂儉僗僷乕僋乯
| 嵶朎幙撪偺捈宎侾亅俀儅僀僋儘儊乕僩儖偺旝彫椞堟偱偺旕揱斃惈偺俠倎俀亄擹搙忋徃丄偡側傢偪僇儖僔僂儉僗僷乕僋偼嵶朎幙撪慡懱偺堦尒儔儞僟儉側抧揰偱敪惗偟傑偡乮恾俈俙丆俛乯丅僇儖僔僂儉僗僷乕僋偺帩懕帪娫偼俁侽亅係侽倣倱倕們偱丄俠倎俀亄擹搙偺僺乕僋傑偱偺帪娫偼栺侾俀倣倱倕們偲怱幒嬝偺僇儖僔僂儉僩儔儞僕僃儞僩偺僺乕僋傑偱偺帪娫偵嬤偄傕偺偱偟偨丅僇儖僔僂儉僗僷乕僋偺敪惗偼 ryanodine 偵傛傝梷惂偝傟傑偟偨偑丄 nicardipine 傗墫壔僇僪儈僂儉乮 俠倓俠倢俀 乯偵偼塭嬁偝傟傑偣傫偱偟偨丅偙傟傜偺惈幙偼僇儖僔僂儉僗僷乕僋偑妶摦揹埵偵埶懚偟側偄俼倄俼俠偐傜偺俠倎俀亄偺帺敪揑曻弌偱偁傞偙偲傪帵偟偰偄傑偡丅 僇儖僔僂儉僗僷乕僋偲僇儖僔僂儉僩儔儞僕僃儞僩偺娭學傪峏偵専摙偡傞偨傔偵怱幒嬝嵶朎偺僇儖僔僂儉僩儔儞僕僃儞僩弶婜憡偺儔僀儞僗僉儍儞夝愅傪峴偄傑偟偨乮恾俉乯丅僇儖僔僂儉僗僷乕僋傪敪惗偟偰偄傞怱幒嬝嵶朎傪揹婥巋寖偟偰僇儖僔僂儉僩儔儞僕僃儞僩傪敪惗偝偣丄倶亅倲昞帵偡傞偲僇儖僔僂儉僗僷乕僋偼棳傟惎偺傛偆偵懆偊傜傟丄偙傟傪侾丏俉儅僀僋儘儊乕僩儖娫妘偱摨帪偵敪惗偝偣傞偲僇儖僔僂儉僩儔儞僕僃儞僩弶婜憡偵側傞傛偆偵尒偊傑偟偨丅堦尒儔儞僟儉偵尒偊偨僇儖僔僂儉僗僷乕僋偺敪惗抧揰偼僇儖僔僂儉僩儔儞僕僃儞僩偱俠倎俀亄擹搙忋徃偑憗偄抧揰丄偮傑傝俿娗偺偁傞抧揰偲堦抳偟偰偄傑偟偨丅偝傜偵丄僇儖僔僂儉僗僷乕僋偑敪惗偟偰偐傜栺俁侽倣倱倕們埲撪偵僇儖僔僂儉僩儔儞僕僃儞僩傪敪惗偝偣偨応崌丄偦偺抧揰偱偺俠倎俀亄曻弌偑寚棊偡傞尰徾偑娤嶡偝傟傑偟偨丅 偙傟傜偺寢壥偼僇儖僔僂儉僗僷乕僋偑俽俼偐傜偺俠倎俀亄曻弌偺嵟彫扨埵偱偁傝丄怱幒嬝偱偼僇儖僔僂儉僗僷乕僋偑嵶朎幙慡懱偱摨帪偵敪惗偟偨傕偺偑僇儖僔僂儉僩儔儞僕僃儞僩偱偁傞偙偲傪帵嵈偟偰偄傑偡丅 儀乕僞傾僪儗僫儕儞庴梕懱巋寖栻偺 isoproterenol 偵傛傝僇儖僔僂儉僗僷乕僋偺敪惗昿搙丄僷僞乕儞丄帪娫宱夁偼塭嬁偝傟傑偣傫偱偟偨偑丄敪惗帪偺僺乕僋俠倎俀亄擹搙乮怳暆乯偑憹戝偟傑偟偨乮恾俈俠乯丅廬棃儀乕僞傾僪儗僫儕儞庴梕懱巋寖偵傛傞怱嬝偺廂弅椡憹戝偼嵶朎枌偐傜偺俠倎俀亄棳擖憹戝偵傛傝愢柧偝傟偰偒傑偟偨丅崱夞娤嶡偝傟偨 isoproterenol 偵傛傞僇儖僔僂儉僗僷乕僋偺怳暆憹戝偼儀乕僞傾僪儗僫儕儞庴梕懱巋寖帪偵俼俽偐傜偺俠倎俀亄曻弌偺嵟彫扨埵曻弌偑廋忺偝傟傞偙偲丄偮傑傝們俙俵俹埶懚惈偺儕儞巁壔摍偵傛傝俼倄俼俠偺婡擻偑曄壔偡傞壜擻惈傪帵嵈偟偰偄傑偡丅尰忬偱偺惗偒偨嵶朎偱俼倄俼俠偺奐岥傪捈愙娤嶡偡傞桞堦偺庤抜偲偟偰丄僇儖僔僂儉僗僷乕僋偼俠倎俀亄曻弌偺惂屼偺尋媶傗栻暔偺奐敪偵墳梡壜擻偱偡丅 |
亂恾俈丂奼戝恾傊亃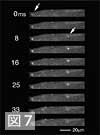 |
亂恾俉丂奼戝恾傊亃 |