 |
東邦大学名誉教授 横山 祐作 |
 麦角アルカロイドの全合成
麦角アルカロイドの全合成  無保護アミノ酸の官能基選択性
無保護アミノ酸の官能基選択性  アミノ酸のラセミ化
アミノ酸のラセミ化
 芳香族アミノ酸のブロム化
芳香族アミノ酸のブロム化  新赤堀反応
新赤堀反応  IDO阻害剤の開発
IDO阻害剤の開発
アミノ酸の化学−新赤堀反応(無保護アミノ酸とアルデヒドの反応)
赤堀反応 : 日本人が1940年代(戦争中)に見つけた反応の再発見!
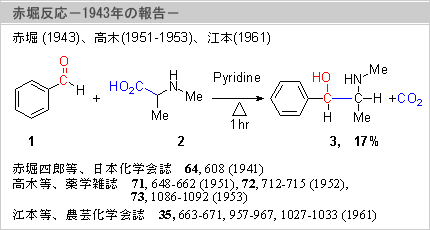
赤堀四郎等は1942年、日本化学会誌にBenzaldehyde(1)とN-Methylalanine(2)をピリジン中加熱することにより、低収率(16%)ながらEphedrine(3)が一行程で得られることを報告した(右図)。その後、高木等が薬学会誌に、江本等は1961年に農芸化学会誌にこの反応を詳細に検討した結果を発表したが、3の収率は10%台以上にはならなかった。この反応は「無保護アミノ酸の脱炭酸と同時のアルキル化」という非常に珍しい反応形式だったばかりでなく、医薬品の基本骨格として多く含まれるアミノアルコールが一行程で得られるという合成法としての意義も大きかった。しかし、これらの報告は、すべて日本語で発表されていたため、世界の注目を浴びることなく埋もれていた。
新赤堀反応−我々の発見−
我々は、これまで検討してきた無保護アミノ酸の合成反応の開発という観点から、この反応に注目し再検討を行った。
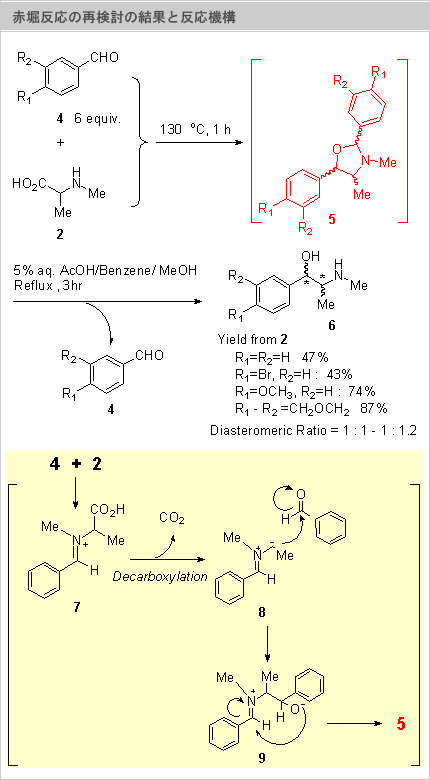
N-Methylalanine(2)と6当量の芳香族アルデヒド(4)とを無溶媒で130℃、1hr加熱したところ、赤堀等の報告と同様に、水層から、エフェドリンは低収率でしか得られなかった。しかし、有機層を精査したところオキサゾリジン体(5)が大量に生成していることがわかった。これを単離することなく5%AcOH水溶液で加水分解したところ、アミノアルコール体(6)がジアステレオマーのほぼ1:1混合物として48%の収率で得られた(右図)。すなわち、赤堀等の実験では、有機層にオキサゾリジン体(5)が生成していたことを、見逃していたため収率が悪かったものと思われる。さらに、この反応を種々の置換ベンズアルデヒドで行ったところ、電子供与基がついたものほど収率は向上し、最高87%の収率で得られた。
また、オキサゾリジン体(5)の生成は、反応機構に関する非常に重要な情報を与えてくれる。すなわち、アミノ酸(2)とアルデヒド(4)が、インミニウム塩(7)を形成し、それが引き金となって脱炭酸がおこり、Zwitter
Ion(8)が生ずる。この8ともう一分子のアルデヒド(4)が反応して生じた9が閉環して、オキサゾリジン体(5)を生成したと考えられる。このオキザゾリジン体(5)は、比較的不安定で酢酸水溶液で加熱すると、加水分解が起こり、アミノアルコール体を与える。
私は、この、日本に埋もれていた独創的な反応が、『赤堀反応』として世界に誇るアミノ酸の新しい有機化学の展開につながるばかりでなく、医薬品の実用合成法として大きな可能性を秘めていると感じている。
これからの課題
1.反応条件の最適化
反応温度、試薬のモル比、添加剤(触媒)の添加等を検討し、出来るだけ緩和な条件下で反応が収率良く進行するようにする。
以下のジアステレオ選択性や立体選択性の問題を解決するためには、この問題の解決は必須である。
2.立体選択的合成(ジアステレオ選択的合成と不斉合成)の開発
現段階では、アミノアルコール体(6)は4種の混合物でえられているが、これらのうち一種類だけを選択的に合成しないと、医薬品合成法としては不十分である。
すなわち、ジアステレオ選択的合成と不斉合成を同時に達成しなければならない。
3.この反応の適用限界
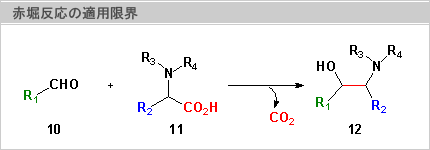
現在の所、この反応はベンズアルデヒド誘導体(4)とN-メチルアラニン(2)との反応しか進行することを確かめていないが、脂肪族アルデヒド(10)や2以外のアミノ酸(11)でも進行すれば、この反応から得られる化合物(12)の種類が多くなり、より多くの医薬品合成に応用できることになる(右図)。すなわち、この反応が有用であることを証明することが出来る。
参考文献:横山祐作、椿 なつめ、山口智嗣、奥野洋明、第32回反応と合成の進歩シンポジウム講演要旨集 (広島) 2006, 224-225.

